Ključna razlika: Atomi so osnovne enote, iz katerih je vsa materija sestavljena. Atomi so majhni, v širini od 0, 1 do 0, 5 nanometrov. Vsak atom katerega koli elementa je sestavljen iz protonov, nevtronov in elektronov. Atomi različnih elementov se združijo in tvorijo molekule. To se zgodi s kemično reakcijo. Molekula je najmanjša količina kemične snovi, ki lahko obstaja.
Element je čista kemična snov, ki ima eno ali eno vrsto atoma, ki se odlikuje po atomskem številu. Atomsko število izhaja iz števila protonov, prisotnih v jedru elementa. Identificiranih je skupaj 118 elementov, razdeljenih med kovino, metaloide in nekovine. Vsak element ima svoj niz lastnosti. Večina elementov je na voljo na Zemlji, nekaj pa jih je umetno razvitih z jedrskimi reakcijami. Element je že v najbolj surovi obliki in ga ni mogoče dodatno razčleniti. Vse elemente lahko najdete v periodnem sistemu, navedenem po atomski številki.
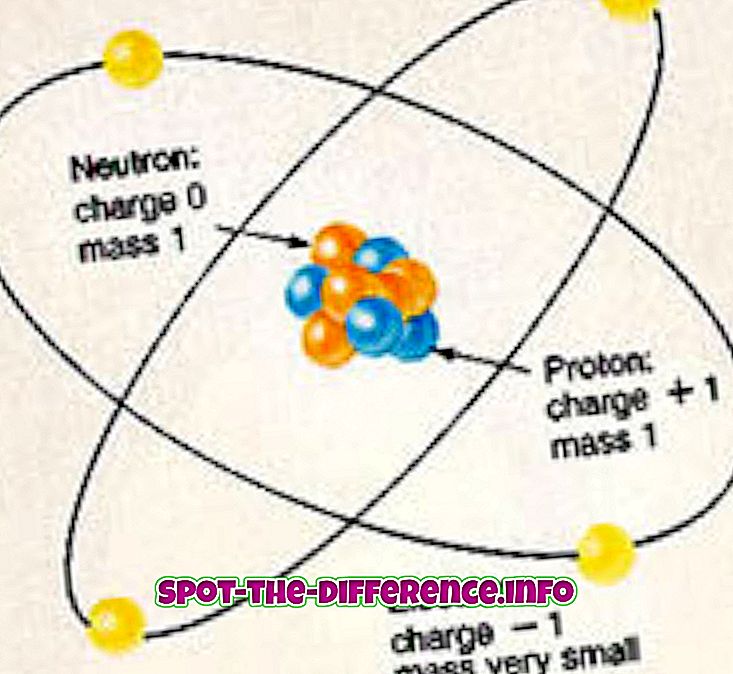
Vsak atom katerega koli elementa je sestavljen iz protonov, nevtronov in elektronov. Protoni in nevtroni tvorijo jedro atoma in se nahajajo v sredini atoma. Jedro je obdano z oblakom elektronov, ki jih elektromagnetna sila veže na jedro. Elektroni imajo negativen naboj, ki ga privlačijo jedra, saj imajo protoni v jedru pozitivni naboj. Po drugi strani pa nevtroni nimajo naboja.
Število protonov, nevtronov in elektronov v atomu določa, kateri element je. Na primer: atom železa ima 26 protonov, 30 nevtronov in 26 elektronov. Vsak atom železa ima to konfiguracijo.
Atomi različnih elementov se združijo in tvorijo molekule. To se zgodi s kemično reakcijo. Na primer: dva atoma vodika in en atom kisika združujeta molekule vode.

Molekula ima lahko zelo različne lastnosti od elementov, iz katerih je narejena. Na primer: voda se obnaša zelo drugače kot kisik ali vodik, čeprav je sestavljena iz dveh vodikovih atomov in enega kisikovega atoma.
Poleg tega atom ne more obstajati neodvisno v naravi, ne da bi se vezal na nekaj. Nikoli ne bomo našli samo enega kisikovega atoma ali enega samega ogljikovega atoma. Vedno je povezan z nečim, kot je O2 (kisik) ali CO2 (ogljikov dioksid). Ko je vezana v molekulo, lahko molekula obstaja v naravi neodvisno, zato lahko vedno najdemo molekulo kisika, molekulo ogljikovega dioksida, molekulo vode (H2O) itd.
V molekuli so atomi zlepljeni skupaj v določeni obliki ali obliki. To je v glavnem odvisno od števila vezi, ki jih lahko povzroči atom. Atomi tvorijo molekule tako, da med seboj tvorijo kemijske vezi. Atomi kisika imajo vedno dve vezi z drugimi atomi, atomi ogljika imajo vedno štiri vezi z drugimi atomi, atomi dušika pa imajo vedno tri vezi z drugimi atomi. Zaradi tega ima določena vrsta molekule vedno določeno obliko, kot je peterokotna, šesterokotna, stranska, dvo-stranska itd.
Molekule vedno težijo k združevanju, njihovi formaciji glede na njihovo stanje. Tako kot v plinastem stanju, so molekule le navdušene. V tekočem stanju so molekule običajno ohlapno združene, tako da se lahko še vedno premikajo. Medtem ko so v trdnem stanju molekule tesno pakirane skupaj in lahko samo vibrirajo.
Molekule so ponavadi predstavljene v molekulski formuli. Na primer: O2, H2O, CO2, C6H12O6 (sladkor). Molekularna formula je ime elementa, ki mu sledi število atomov elementa v molekuli.