Ključna razlika: Kisline in baze so dve vrsti jedkih snovi. Vsaka snov s pH vrednostjo med 0 in 7 se šteje za kislo, medtem ko je pH vrednost 7 do 14 osnova. Kisline so ionske spojine, ki se v vodi razgrajujejo, da tvorijo vodikov ion (H +). Ionske spojine so spojina s pozitivnim ali negativnim nabojem. Baze, na drugi strani, so ionske spojine, ki se v vodi razgradijo in tvorijo negativno nabiti hidroksidni ion (OH-).

Vse kemijske spojine imajo pH vrednost. Merilo pH je od 0 do 14. To je merilo koncentracije vodikovih ionov v raztopini. Vsaka snov nad nevtralnim pH se šteje za bazo, medtem ko se katera koli snov pod nevtralnim pH šteje za kislino. Nevtralni pH je pH čiste vode, tj. 7. Vsaka snov s pH vrednostjo med 0 in 7 se šteje za kislo, medtem ko je pH vrednost 7 do 14 osnova.
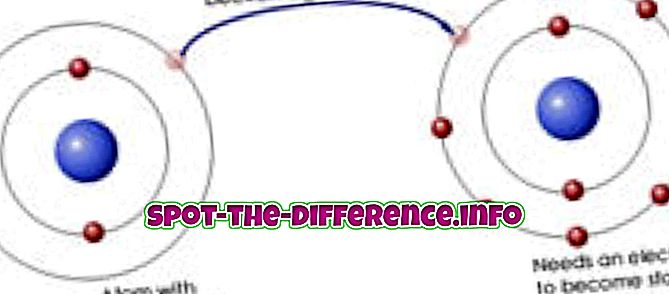
Kisline so ionske spojine, ki se v vodi razgrajujejo, da tvorijo vodikov ion (H +). Ionske spojine so spojina s pozitivnim ali negativnim nabojem. Baze, na drugi strani, so ionske spojine, ki se v vodi razgradijo in tvorijo negativno nabiti hidroksidni ion (OH-). Jakost kisline ali baze je določena na podlagi tega, koliko njihovih ionov se sprosti; več ionov so močnejši.
Poleg tega, če se kombinirajo kisline in baze enake jakosti, nastanejo sol in voda. Na primer: HCl (kislina) + NaOh (baza) = NaCl (sol za gospodinjstvo) + H2O (voda)
Značilnosti kislin:
- okusite kislo, ko se jedo
- kožo lahko kožo kožemo
- lahko korodira (ali izžre) kovine in kožo
- lahko uporabimo kot reaktant med elektrolizo zaradi prisotnosti mobilnih ionov
- obrnite modro lakmusovo rdečo
- študirajo v kemiji in biologiji
- na univerzalnem indikatorju postane rdeča ali oranžna
Kisline lahko razvrstimo v:
- Močne kisline - najpogostejše so žveplova kislina, dušikova kislina in klorovodikova kislina (H2SO4, HNO3 oziroma HCl).
- Nekatere koncentrirane šibke kisline, na primer mravljinčna kislina in ocetna kislina
- Močne Lewisove kisline, kot je brezvodni aluminijev klorid in borov trifluorid
- Lewisove kisline s specifično reaktivnostjo, npr. Raztopine cinkovega klorida
- Izjemno močne kisline (superkisline)

- Grenak okus (v nasprotju s kislim okusom kislin)
- Slimy ali sapunico na prstih
- Veliko baz reagira s kislinami in precipitirajo soli.
- Močne baze lahko burno reagirajo s kislinami. Razlitje kisline lahko varno nevtralizirate z uporabo blage baze.
- Osnove obarvajo rdečo lakmusovo papir modro
- Osnove so snovi, ki vsebujejo kovinske okside ali hidrokside
- Baze, ki so topne v vodi, tvorijo alkalije (topne baze)
Osnove lahko razvrstimo v:
- Kavstične snovi ali alkalije, kot so natrijev hidroksid (NaOH) in kalijev hidroksid (KOH)
- Alkalne kovine v kovinski obliki (npr. Natrijev element) in hidridi alkalijskih in zemeljskoalkalijskih kovin, kot je natrijev hidrid, delujejo kot močne baze in hidrirajo, da dajejo kaustiko
- Izjemno močne baze (superfaze), kot so alkoksidi, kovinski amidi (npr. Natrijev amid) in organokovinske baze, kot je butillitij
- Nekatere koncentrirane šibke baze, kot je amoniak, kadar je brezvoden ali v koncentrirani raztopini
Acid | Base | |
Arrhenius Definicija | Kislina je katera koli kemična spojina, ki pri raztopitvi v vodi daje raztopino z aktivnostjo vodikovih ionov večjo kot v čisti vodi. | Osnova je vodna snov, ki lahko sprejme vodikove ione. |
Bronstead Lowry Definicija | Kislina je snov, ki daje proton. | Osnova je vsaka snov, ki sprejme proton. |
pH vrednost | Manj kot 7, 0 | Več kot 7, 0 |
Lakmusov papir | Modri lakmusov papir postane rdeč | rdeči lakmusov papir postane modri |
Fenolftalein | Ostaja brezbarven | Raztopina postane roza |
Disociacija (v vodi) | Kisle proste vodikove ione (H +), kadar so zmešane z vodo. | Pri mešanju z vodo bazne proste hidroksidne ione (OH-). |
Kemična formula | Kislina ima kemijsko formulo s H na začetku. Na primer HCl (klorovodikova kislina). Obstaja ena izjema od njegovega pravila, CH3COOH = ocetna kislina (kis). | Osnova ima na koncu kemijske formule z OH. Na primer NaOH (natrijev hidroksid). |